Лекарства, используемые при реанимации и некоторых неотложных состояниях
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Для восстановления самостоятельного кровообращения необходимо как можно раньше начать введение медикаментозных препаратов и инфузионную терапию. Перечень препаратов, в настоящее время используемых при проведении первичных реанимационных мероприятий, относительно невелик.

Адреналин
Адреномиметик, наиболее часто используемый при проведении сердечно-легочной и церебральной реанимации. Улучшает коронарный и мозговой кровоток, повышает возбудимость и сократимость миокарда, сужает периферические сосуды.
Цель терапии — достижение спонтанной и стабильной гемодинамики при систолическом давлении не менее 100-110 мм рт. ст. Способствует восстановлению ритма при асистолии и электромеханической диссоциации, а также переводу мелковолновой фибрилляции желудочков в крупноволновую.
Первичная доза адреналина составляет 1 мг (1 мл 0,1 % раствора) внутривенно. Интервалы между введением адреналина составляют от 3 до 5 минут. При внутритрахеальном введении доза адреналина составляет 3 мг (на 7 мл изотонического раствора хлорида натрия).
После восстановления сердечной деятельности существует высокий риск рецидива фибрилляции желудочков, обусловленной неадекватной коронарной перфузией. По этой причине адреналин используют в качестве инотропной поддержки в дозе 1-10 мкг/мин.

Вазопрессин
Вазопрессин (антидиуретический гормон — АДГ) — гормон задней доли гипофиза. Секретируется при повышении осмолярности плазмы крови и при уменьшении объема внеклеточной жидкости.
Увеличивает реабсорбцию воды почками, повышая концентрацию мочи и уменьшая ее выделяемый объем. Имеет также ряд эффектов на кровеносные сосуды и головной мозг.
По результатам экспериментальных исследований вазопрессин способствует восстановлению сердечной деятельности и коронарной перфузии.
На сегодняшний день вазопрессин рассматривается как возможная альтернатива адреналину.
Установлено, что уровень эндогенного вазопрессина значительно выше у лиц, успешно реанимированных, в сравнении с умершими.
Вводится вместо первого или второго введения адреналина однократно внутривенно в дозе 40 мг. При неэффективности повторно не применяется — рекомендуется переход на введение адреналина.
Несмотря на многообещающие результаты исследований, в многоцентровых исследованиях не было выявлено повышения госпитальной выживаемости при использовании вазопрессина. Поэтому Международный Консенсус 2005 г. заключил, что «в настоящее время нет убедительных доказательств как за, так и против использования вазопрессина в качестве альтернативы или в комбинации с адреналином при любом ритме сердца во время СЛР».
Кордарон
Антиаритмический препарат III класса (ингибитор реполяризации). Обладает также антиангинальным, коронародилатирующим, альфа- и бета-адреноблокирующим, а также гипотензивным действием. Антиангинальный эффект препарата обусловлен коронарорасширяющим, антиадренергическим действием и уменьшением потребности миокарда в кислороде.
Оказывает тормозящее влияние на альфа- и бета-адренорецепторы без развития их полной блокады. Уменьшает чувствительность к гиперстимуляции симпатической нервной системы, снижает тонус коронарных сосудов, увеличивает коронарный кровоток; урежает частоту сердечных сокращений и повышает энергетические резервы миокарда (за счет увеличения содержания креатинсульфата, аденозина и гликогена). Снижает общее периферическое сопротивление и системное артериальное давление при внутривенном введении. Антиаритмическое действие обусловлено влиянием на электрофизиологические процессы в миокарде, удлиняет потенциал действия кардиомиоцитов, увеличивая эффективный рефрактерный период предсердий, желудочков, AV-узла, пучка Гиса и волокон Пуркинье, добавочных путей проведения возбуждения. Блокируя инактивированные «быстрые» натриевые каналы, оказывает эффекты, характерные для антиаритмических средств I класса. Тормозит медленную (диастолическую) деполяризацию мембраны клеток синусного узла, вызывая брадикардию, угнетает АV-проведение (эффект антиаритмиков IV класса).
Эффективность кордарона при проведении реанимационных мероприятий подтверждена во многих исследованиях. Считается препаратом выбора у пациентов с фибрилляцией желудочков и желудочковой тахикардией, рефрактерными к трем начальным разрядам дефибриллятора.
Вводится внутривенно болюсно в дозе 300 мг на 20 мл 5% глюкозы. Дополнительно рекомендуется проводить поддерживающую инфузию из расчета 1 мг/мин -1 в течение 6 часов (затем 0,5 мг/мин -1 ). Возможно дополнительное введение 150 мг препарата, если имеет место рецидив фибрилляции желудочков или желудочковой тахикардии.
Гидрокарбонат натрия
Является буферным раствором (рН 8,1), используемым для коррекции нарушений кислотно-основного состояния.
Применяют в виде 4,2 и 8,4% раствора (8,4% раствор бикарбоната натрия называется молярным, так как в 1 мл содержится 1 ммоль Na и 1 ммоль НСО2).
В настоящий момент использование гидрокарбоната натрия во время проведения реанимации ограничено в связи с тем, что неконтролируемое введение препарата может вызвать метаболический алкалоз, приводить к инактивации адреналина и снижению эффективности электрической дефибрилляции.
Не рекомендуется применять его до восстановления самостоятельной работы сердца. Это связано с тем, что ацидоз при введении гидрокарбоната натрия будет уменьшен лишь в случае удаления через легкие образующегося при его диссоциации СО2. В случае же неадекватности легочного кровотока и вентиляции СО2 усиливает вне- и внутриклеточный ацидоз.
Показанием к введению препарата считают гиперкалиемию, метаболический ацидоз, передозировку трициклических антидепрессантов и антидепрессантов. Гидрокарбонат натрия вводят в дозе 0,5-1,0 ммоль/кг, если процесс реанимации затягивается свыше 15-20 минут.

Хлористый кальций
Использование препаратов кальция при сердечно-легочной реанимации ограничено в связи с возможным развитием реперфузионных поражений и нарушением продукции энергии.
Введение препаратов кальция при проведении реанимационных мероприятий показано при наличии гипокальциемии, гиперкалиемии и передозировке антагонистов кальция.
Вводится в дозе 5-10 мл 10% раствора (2-4 мг/кг или) за 5-10 минут (10 мл 10% раствора содержит 1000 мг препарата).

Атропина сульфат
Атропина сульфат относится к группе антихолинергических лекарственных средств. Способность атропина связываться с холинорецепторами объясняется наличием в его структуре фрагмента, роднящего его с молекулой эндогенного лиганда — ацетилхолина.
Основная фармакологическая особенность атропина — его способность блокировать М-холинорецепторы; он действует также (хотя значительно слабее) на Н-холинорецепторы. Атропин относится, таким образом, к неизбирательным блокаторам М-холинорецепторов. Блокируя м-холинорецепторы, он делает их нечувствительными к ацетилхолину, образующемуся в области окончаний постганглионарных парасимпатических (холинергических) нервов. Понижает тонус блуждающего нерва, повышает атриовентрикулярную проводимость проводимость, уменьшает вероятность развития желудочковой фибрилляции вследствие гипоперфузии при выраженной брадикардии, увеличивает частоту сердечных сокращений при AV-блокаде (кроме полного АV-блока). Применение атропина показано при асистолии, сердечной активности без пульса при частоте сердечных сокращений менее 60, а также при брадисистолии*.
* Согласно рекомендациям ERC и AHA 2010 г., атропин не рекомендован для терапии электромеханической диссоциации/асистолии и исключен из алгоритма интенсивной терапии по поддержанию сердечно-сосудистой деятельности при остановке сердца.
В настоящее время нет убедительных данных о том, что атропин играет значимую роль при лечении асистолии. Тем не менее, в рекомендациях ERC и AHA 2005 г. препарат был рекомендован к использованию, так как прогноз при лечении асистолии чрезвычайно неблагоприятный. В связи с этим использование атропина не может еще более ухудшить ситуацию.
Рекомендуемая доза при асистолии и электрической активности без пульса с частотой сердечных сокращений менее 60 в минуту составляет 3 мг. Препарат вводится однократно. Рекомендации по кратности введения препарата в настоящее время изменились: предлагается ограничить его введение однократной дозой в 3 мг внутривенно. Эта доза достаточна для блока вагусной активности у взрослых пациентов. В ампуле 1 мл 0,1 % раствора атропина содержится 1 мг препарата.

Лидокаин
Антиаритмическая активность препарата обусловлена угнетением фазы 4 (диастолической деполяризации) в волокнах Пуркинье, уменьшением автоматизма и подавлением эктопических очагов возбуждения. На скорость быстрой деполяризации (фаза 0) не влияет или незначительно снижает ее. Увеличивает проницаемость мембран для ионов калия, ускоряет процесс реполяризации и укорачивает потенциал действия. Не изменяет возбудимость синусно-предсердного узла, мало влияет на проводимость и сократимость миокарда. При внутривенном введении действует быстро и коротко (10-20 мин).
Лидокаин повышает порог развития фибрилляции желудочков, купирует желудочковую тахикардию, способствует переводу желудочковой фибрилляции в желудочковую тахикардию, эффективен при желудочковых экстрасистолиях (частые, политопные, групповые экстрасистолы и аллоритмии).
В настоящее время рассматривается как альтернатива кордарону только при недоступности последнего. Нельзя вводить лидокаин после введения кордарона. Сочетанное введение этих двух препаратов приводит к реальной угрозе потенцирования сердечной слабости и проявления проаритмического действия.
Вводится нагрузочная доза лидокаина 80-100 мг (1,5 мг/кг) внутривенно струйно. После достижения самостоятельного кровообращения проводится поддерживающая инфузия лидокаина в дозе 2-4 мг/мин.
Сульфат магния
Сульфат магния обладает антиаритмическим эффектом при нарушениях водно-электролитного баланса (гипомагниемия и др.). Магний — важная составляющая ферментных систем организма (процесс образования энергии в мышечной ткани), необходим для осуществления нейрохимической трансмиссии (угнетение выброса ацетилхолина и снижение чувствительности постсинаптических мембран).
Используется как дополнительное антифибрилляторное средство при остановке кровообращения на фоне гипомагниемии. Средство выбора при желудочковой тахикардии torsades de pointes — пируэтная тахикардия (рис. 4.1).
Гипомагниемия часто сочетается с гипокалиемией, что также может служить причиной остановки сердечной деятельности.
Сульфат магния вводится болюсно 1-2 г внутривенно в течение 1-2 минут. При недостаточности эффекта показано повторное введение в той же дозе через 5-10 минут (в ампуле 10 мл 25% содержится 2,5 г препарата).

Растворы глюкозы
В настоящее время не рекомендуется использовать инфузию глюкозы при проведении реанимационных мероприятий в связи с тем, что она поступает в ишемизированную область мозга, где, включаясь в анаэробный обмен, расщепляется до молочной кислоты. Локальное накопление в мозговой ткани лактата увеличивает ее повреждение. Более предпочтительно использование физиологического раствора или раствора Рингера. После реанимационных мероприятий надо строго следить за уровнем глюкозы в крови.
Для определения пограничного уровня глюкозы, требующего введения инсулина, а также допустимых колебаний целевой концентрации глюкозы в крови, необходимы дальнейшие исследования.
Источник статьи: http://ilive.com.ua/health/lekarstva-ispolzuemye-pri-reanimacii-i-nekotoryh-neotlozhnyh-sostoyaniyah_106671i15828.html
Сердечно-легочная реанимация на догоспитальном этапе
Каковы наиболее частые причины внезапной смерти? Что можно сделать в случаях остановки дыхания и кровообращения на догоспитальном этапе? Почему внутрисердечный путь введения лекарственных средств — «путь отчаяния»? Сердечно-легочная реанимация — э
Каковы наиболее частые причины внезапной смерти?
Что можно сделать в случаях остановки дыхания и кровообращения на догоспитальном этапе?
Почему внутрисердечный путь введения лекарственных средств — «путь отчаяния»?
Сердечно-легочная реанимация — это комплекс мероприятий, направленных на оживление организма в случае остановки кровообращения и/или дыхания. Своевременное (в течение первых минут) начало реанимационных мероприятий может предотвратить необратимое повреждение мозга и, возможно, наступление биологической смерти.
Большинство случаев внезапной смерти имеют кардиальную причину.
Основными признаками остановки кровообращения являются потеря сознания, остановка дыхания и отсутствие пульса (следует оценивать наличие пульса на сонных артериях).
Сердечно-легочная реанимация (СРЛ) состоит из двух основных частей.
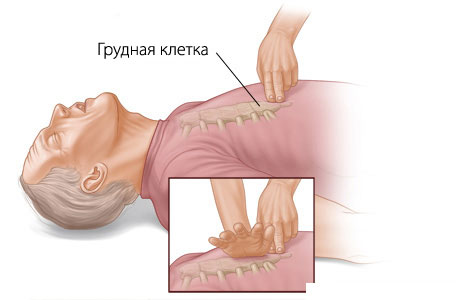
- Основные реанимационные мероприятия (ОРМ) или неспецифическая реанимация. Проводится вне зависимости от причины остановки кровообращения и включает в себя поддержание кровообращения (наружный массаж сердца с частотой 80—100 компрессий в минуту следует производить, положив больного на твердую поверхность), а также обеспечение проходимости дыхательных путей и достаточного уровня вентиляции легких (искусственная вентиляция легких — 12 вдохов в минуту методами «рот в рот», «рот в нос» или с помощью дыхательного мешка). Начинать реанимацию следует со вдоха, а затем, в том случае если реанимацию проводит один человек, осуществлять 12—15 компрессий на 2 вдоха, если же два человека — 5 компрессий на один вдох. Вероятность сохранения жизни пациента в случае остановки кровообращения обратно пропорциональна времени, прошедшему до момента начала реанимационных мероприятий.
Алгоритм действий при проведении ОРМ представлен на рис. 1.
- Специализированные реанимационные мероприятия — использование лекарственных средств и реанимационного оборудования в зависимости от причин, вызвавших остановку кровообращения. Эти мероприятия не исключают, а дополняют ОРМ.
Способы введения лекарственных препаратов при СЛР
Внутривенный. При налаженном периферическом венозном доступе возможно введение лекарственных препаратов в периферическую вену, но после каждого болюсного введения необходимо поднимать руку больного для ускорения доставки препарата к сердцу, сопровождая болюс введением некоторого количества жидкости (для его проталкивания). С целью обеспечения доступа в центральную вену предпочтительно катетеризировать подключичную или внутреннюю яремную вену. Введение лекарственных препаратов в бедренную вену сопряжено с их замедленной доставкой к сердцу и уменьшением концентрации.
Эндотрахеальный. Если интубация трахеи произведена раньше, чем обеспечен венозный доступ, то атропин, адреналин, лидокаин можно вводить зондом в трахею. При этом препарат разводят на 10 мл физиологического раствора, и его доза должна быть в 2–2,5 раза больше, чем при внутривенном введении. Конец зонда должен находиться ниже конца интубационной трубки; после введения препарата необходимо выполнить последовательно 2—3 вдоха (прекратив при этом непрямой массаж сердца) для распределения лекарства по бронхиальному дереву.
Внутрисердечный. «Путь отчаяния» применяется лишь в том случае, если невозможен другой способ введения. Следует по возможности воздерживаться от внутрисердечных инъекций, так как при использовании этого способа в 40% случаев повреждаются крупные коронарные артерии.
Тактика реанимации при фибрилляции желудочков и гемодинамически неэффективной желудочковой тахикардии
Начинать реанимацию необходимо с ОРМ и электрической дефибрилляции (ЭДФ). Дефибрилляцию начинают с разряда мощностью 200 Дж. При сохранении фибрилляции снова используют разряд, но более высокой мощности — 200—300 Дж, затем — 360 Дж. Начинать реанимационные мероприятия сразу с разряда максимальной мощности не следует, чтобы избежать повреждающего действия на миокард.
При неэффективности вышеперечисленных мероприятий возобновляют ОРМ, производят интубацию трахеи, налаживают венозный доступ, вводят адреналин в дозе 1 мг каждые 3—5 минут; можно вводить возрастающие дозы адреналина 1—3—5 мг каждые 3—5 минут или промежуточные дозы 2—5 мг каждые 3—5 минут. Адреналин можно заменить вазопрессином, который вводится в дозировке 40 мг в вену однократно.
При продолжении фибрилляции желудочков используют антиаритмические препараты, которые позволяют снизить порог дефибрилляции:
- лидокаин 1,5 мг/кг внутривенно струйно, повторное введение через 3-5 минут, в случае восстановления кровообращения налаживают непрерывную инфузию лидокаина со скоростью 2-4 мг/мин;
- амиодарон 300 мг в вену за 2-3 минуты, при отсутствии эффекта возможно введение еще 150 мг в вену; в случае восстановления кровообращения налаживают непрерывную инфузию в первые 6 часов 1мг/мин (360 мг), в следующие 18 часов 0,5 мг/мин (540 мг);
- прокаинамид в дозировке 100 мг; при необходимости введение повторяют через 5 минут (до общей дозы 17 мг/кг);
- сульфат магния 1-2 г в течение 5 минут, при необходимости введение можно повторить через 5-10 минут при тахикардии «пируэт».
После введения лекарства 30—60 секунд проводят ОРМ, а затем повторно проводят ЭДФ (за это время антиаритмик достигает цели). Рекомендуется чередовать введение лекарств с ДФ по такой схеме: антиаритмик — ЭДФ (360 кДж) — адреналин — ЭДФ (360 кДж) —антиритмик — ЭДФ (360 кДж) — адреналин и т. д. Можно использовать не один, а три разряда максимальной мощности. Количество ЭДФ не ограничено.
Алгоритм действий при фибрилляции желудочков представлен на рис. 2.
Широко практиковавшееся ранее введение бикарбоната натрия (как средства борьбы с ацидозом) в настоящее время применяется значительно реже из-за ограниченных показаний:
- затянувшиеся (более 15 минут) реанимационные мероприятия;
- отравление трициклическими антидепрессантами;
- выраженный ацидоз;
- гиперкалиемия.
Бикарбонат натрия вводится в дозе 1 мэкв/кг в вену (в среднем 140–180 мл 4%-ого раствора).
Тактика при электромеханической диссоциации
Электромеханическая диссоциация (ЭМД) — это отсутствие пульса и дыхания у больного с сохраненной электрической активностью сердца (на мониторе ритм виден, а пульса нет).
К сожалению, прогноз при этом виде нарушения деятельности сердца плохой, если не устраняется причина, вызвавшая остановку кровообращения (ацидоз, гиповолемия, гипоксия, гипотермия, тампонада сердца, напряженный пневмоторакс).
Лечение ЭМД включает ОРМ, внутривенное введение адреналина — 1 мг каждые 3—5 минут и атропина 1 мг каждые 3—5 минут, электрокардиостимуляцию, на 15-й минуте реанимации введение бикарбоната натрия. Необходимо попытаться устранить причину ЭМД.
Тактика при асистолии
Тактика устранения этой причины остановки кровообращения практически не отличается от схемы лечения ЭМД. Необходимо обратить внимание на то, что ЭКГ в одном отведении при мелковолновой фибрилляции желудочков может имитировать экстрасистолию, поэтому асистолия должна быть подтверждена в нескольких отведениях ЭКГ. Электрическая дефибрилляция в этом случае не только не показана, но даже вредна, так как она усиливает ваготонию. Лечение включает ОРМ, в вену вводится адреналин — 1 мг каждые 3—5 минут, атропин — 1 мг каждые 3—5 минут, проводится электрокардиостимуляция, на 15-й минуте реанимации показано введение бикарбоната натрия. Необходимо попытаться устранить причину асистолии. Алгоритм действий при асистолии представлен на рис. 3.
Заключение
В случае успешно проведенных реанимационных мероприятий необходимо:
- убедиться в том, что имеет место адекватная вентиляция легких (проходимость дыхательных путей, симметричность дыхания и экскурсии грудной клетки; оценить цвет кожных покровов, при наличии пульсоксиметра убедиться, что сатурация кислородом составляет не менее 90%);
- продолжить введение антиаритмиков с профилактической целью;
- попытаться выявить, какое патологическое состояние привело к остановке кровообращения, и начать лечение основного заболевания.
А. Л. Верткин, доктор медицинских наук, профессор
О. Б. Талибов, кандидат медицинских наук
О. Н. Ткачева
МГМСУ, ННПОСМП, Москва
Источник статьи: http://www.lvrach.ru/2002/12/4529905
Проведение сердечно-легочной реанимации
Современные протоколы проведения СЛР
В 2005 году были приняты международные рекомендации (International Liaison Committee on Resuscitation) по проведению СЛР.
Протокол сердечно-легочной реанимации 2005 года
В основном изменения коснулись первичного реанимационного комплекса. Они направлены на упрощение процедуры СЛР для реаниматоров. Для проведения СЛР реаниматор помещает руки в центре груди. Соотношение вдох/компрессия должно быть 2:30, вне зависимости от количества человек, проводящих сердечно-легочную реанимацию. Каждый спасательный вдох осуществляется за 1 секунду, а не за 2 секунды;
В начале СЛР двух «спасательных» вдохов не проводится, а сразу приступают к компрессии сердца. Не задерживайте проведение дефибрилляции, если СЛР проводится в условиях стационара. Если сердечный ритм после дефибрилляции не восстанавливается, не проводится серия из трех повторных разрядов большей мощности, а незамедлительно приступают к выполнению массажа сердца. Следующие попытки дефибрилляции проводятся только после 2 минут реанимации (т.е. приблизительно после 5 циклов дыхание/компрессия 2:30).
Если есть сомнение относительно того, является ли ритм асистолией или мелко-волновой фибрилляцией желудочков, следует не пытаться осуществлять дефибрилляцию. Вместо этого продолжать компрессии грудной клетки и искусственное дыхание. Начальная энергия дефибрилляции бифазных дефибрилляторов 150-200 J. Для второго и последующих разрядов – 150-360 J. Энергия монофазных дефибрилляторов – 360 J для первого и последующих разрядов.
Если доказано, или подозревается, что причиной остановки сердца является тромбоэмболия легочной артерии (ТЭЛА), а стандартная СЛР неэффективна, необходимо рассмотреть возможность проведения тромболитической терапии. Если тромболитики были использованы, СЛР необходимо проводить в течение 60-90 мин.
СЛР у детей
Соотношение вдох/компрессия должно быть 2:30, если сердечно-легочную реанимацию проводит один реаниматор. Соотношение вдох/компрессия должно быть 2:15, если сердечно-легочную реанимацию проводят два реаниматора.
Протокол сердечно-легочной реанимации 2010 года
На сегодняшний день большинство отечественных и зарубежных специалистов ориентируется на рекомендации 2010 г Американской ассоциации сердечных заболеваний по проведению СЛР. Они являются дальнейшим развитием рекомендаций 2005 г и содержат целый ряд важных уточнений.
Остановимся на наиболее значимых. Предложено заменить последовательность основных мероприятий по поддержанию жизнедеятельности A-B-C (освобождение дыхательных путей, искусственное дыхание, компрессионные сжатия) последовательностью C-A-B (компрессионные сжатия, освобождение дыхательных путей, искусственное дыхание) для взрослых, детей и грудных детей.
Подчеркивается важность качественного выполнения СЛР: компрессия грудной клетки должна выполняться с надлежащей частотой (не менее 100 сжатий в минуту), амплитудой (для взрослых 5-6 см) и с полным расправлением грудной клетки после каждого сжатия. Следует избегать гипервентиляции во время проведения СЛР. Рекомендуется ЧД – 8-10 в 1 минуту, дыхательный объем – 6-8 мл/кг идеальной массы тела больного.
Интубированным пациентам проводится количественная капнография на протяжении всего периода остановки сердца. Капнография позволяет подтвердить положение эндотрахеальной трубки, контролировать качество выполнения СЛР и объективно подтвердить восстановление спонтанного кровообращения. Если значение PetCO2 70 мм рт. ст. , SрO2 > 92%) крови используйте 100% кислород.
Определить параметры гемодинамики (АД, ЧСС, ЦВД). Осуществить надежный венозный доступ (катетеризация периферических или центральных вен). Оцените степень неврологического дефицита (по шкале комы Глазго), соматическое состояние пациента. Назначьте необходимые инструментальные (рентгенография органов грудной клетки, ЭКГ, эхокардиография и др.) и лабораторные исследования.
Базисные мероприятия
Проводятся до выхода больного из тяжелого состояния. Терапия должна быть направлена на достижение следующих параметров гомеостаза:
- РаO2 > 70 мм рт. ст., а РаСO2 в пределах 35-40 мм рт. ст;
- PetСO2 36-45 мм рт. ст;
- Насыщение гемоглобина смешанной венозной крови кислородом (ScvO2) > 70%;
- Доставка кислорода > 600 мл/(мин-м2);
- Центральное венозное давление (CVP) от 8 до 12 мм рт. ст;
- Систолическое АД в пределах 120-160 мм рт. ст;
- Среднее артериальное давление 65-90 мм рт.ст;
- Уровень глюкозы в крови 3,4-10 ммоль/л;
- Натрий крови 137-145 ммоль/л;
- Осмолярность 285-295 мосм/л;
- Гематокрит > 30%, Нb > 80 г/л;
- Температура тела не более 37,5°C;
- Лактат 0,5 мл/кг/ч;
Приподнятое положение головного конца кровати на 20-45 градусов – после стабилизации гемодинамики.
Профилактика нарушений ритма
В тех случаях, когда остановка сердца была вызвана фибрилляцией желудочков или желудочковой тахикардией, введите внутривенно 300-900 мг (суточная доза) амиодарона.
Группа с предполагаемым благоприятным исходом
Если после короткой СЛР быстро восстановилась сердечная деятельность и дыхание, гемодинамика стабильна, в течение 20 минут восстановилось ясное сознание или имеется неглубокий сопор (13-15 баллов ШГ), но пациент правильно отвечает на вопросы, мероприятия по лечению постреанимационной болезни сводятся к минимуму.
Обычно назначается умеренная седативная терапия (бензодиазепины), про-одится профилактика нарушений ритма сердца, устанавливается динамическое наблюдение за больным (обязательно – ЭКГ-мониторинг), проводится лечение заболевания или состояния, которые явилась причиной остановки сердца.
Группа, с неясным, или с, возможно, неблагоприятным исходом
Часто сознание больного спустя 20 минут после СЛР остается нарушенным. Не только пациенты, находящиеся в коме, но и пациенты, не способные осмысленно реагировать на голосовые команды, должны быть включены в эту группу. Заметим, что неврологический прогноз для этой группы не слишком оптимистичен – только 3-20% из оживленных пациентов могут возобновить свой прежний образ жизни.
Эти пациенты требуют использования всего арсенала профилактических и восстановительных средств, которые имеются в распоряжении врача. Центральное место в этом списке занимает умеренная гипотермия – именно ее применение позволило улучшить исходы и процент выживших больных после СЛР.
Считается, что ранняя оценка неврологического статуса не позволяет судить о прогнозе. Тем не менее, кома 3-6 баллов по ШГ, наличие судорог в первый час после реанимации предполагают плохой прогноз. Если кома сохраняется в течение 48 часов, вероятность плохого неврологического прогноза очень высока. При сохранении глубокой комы (≤ 5 ШГ) спустя 72 часа после остановки кровообращения, в дальнейшем практически у всех больных развивается персистирующее вегетативное состояние.
У многих пациентов этой группы развиваются нарушения гемодинамики. В большинстве случаев причиной является системная воспалительная реакция (SIRS). Гипотензия в основном обусловлена вазодилатацией. Патогенез этого состояния очень напоминает патогенез септического шока. Реже гипотензия связана со снижением сократимости миокарда – например, вследствие инфаркта миокарда, декомпенсации ХСН, миокардита и т.д.
Лечение
Искусственная вентиляция легких
ИВЛ должна начаться немедленно, как только медики установили, что пациент соответствует группе с неясным, или с, возможно, неблагоприятным исходом. Используют режимы искусственной вентиляции легких, которые позволяют поддерживать достаточную оксигенацию крови и избежать повышения внутричерепного давления – насыщение артериальной крови кислородом 94% до 96%, РаO2 > 70 8 баллов, ИВЛ прекращают.
Седативная терапия
Седативная терапия позволяет уменьшить потребление мозгом кислорода, метаболические потребности организма, синхронизировать больного с аппаратом ИВЛ. Большинство препаратов, используемых для седации, обладают противосудорожной активностью.
Внимание. Практически во всех случаях следует сочетать введение наркотических анальгетиков (морфин, фентанил) и гипнотиков (пропофол, мидазолам, диазепам).
Из-за лучшей управляемости удобнее всего использовать в/в инфузию пропофола. Бензодиазепины (одни, или в сочетании с наркотическими анальгетиками) более доступны и широко применяются для этих целей. Дозировки подбирают индивидуально, ориентируясь на общепринятые критерии: ликвидация психомоторного возбуждения, синхронизация с аппаратом ИВЛ, уменьшение тахикардии, стабилизация АД и т.д.
Барбитураты в настоящее время рекомендуется назначать только как средство для контроля повышенного ВЧД, или для лечения резистентного к обычной терапии судорожного синдрома. Обычно, как уже упоминалось выше, через сутки проведение седативной терапии прекращают и оценивают неврологический статус больного.
Лечебная гипотермия
Использование умеренной гипотермии после СЛР на протяжении 12-24 часов, достоверно улучшает прогноз для жизни у больных с остановкой сердца. На сегодняшний день применение терапевтической гипотермии рассматривается как стандарт лечения коматозных пациентов после остановки сердца. Чем раньше будет достигнут оптимальный температурный уровень (центральная температура 32-34°C), тем лучше исходы. По оценке специалистов, каждый час задержки с выполнением гипотермии приводит приблизительно к 20% увеличению смертности.
Противопоказанием служат: наличие глубокой гипотонии, необходимость использовать высокие дозы вазопрессоров для поддержания гемодинамики, бесперспективность реанимационных мероприятий, коагулопатии.
Блокирование центра теплорегуляции
Дрожь – естественная реакция организма на охлаждение, увеличивает скорость обмена веществ и предотвращает или замедляет достижение заданной температуры. Обычно наблюдается при изменении температуры от 37°С к 35°C. При более низкой температуре дрожь обычно прекращается. Седация должна предотвратить возникновение дрожи и блокировать центр терморегуляции, но для этого она должна быть достаточно глубокой. Следует также обратить внимание, что гипотермия снижает клиренс седативных средств, анальгетиков, мышечных релаксантов.
Внимание. Фактически должна проводиться самая обычная общая внутривенная анестезия с использованием наркотических анальгетиков (фентанил), мышечных релаксантов, гипнотиков (пропофол). При этом пациент, пусть медленно, будет пассивно охлаждаться, даже если не принимать специальных мер. Магния сульфат эффективно устраняет дрожь. Вызывая периферическую вазодилатацию, увеличивает скорость теплоотдачи. Вводят в/в 4-5 г магния сульфата за 10-20 минут. Затем в/в инфузия со скоростью 1-2 г/ч, пока температура пациента не снизится до 33°C.
Методика проведения гипотермии
Всем пациентам, которым планируется использовать гипотермию, требуется проведение искусственной вентиляции легких. Определенная проблема заключается в том, как при отсутствии специальной аппаратуры для гипотермии быстро снизить температуру тела до оптимального уровня.
Рекомендуется такой порядок действий:
1. Внутривенно вводится приблизительно 20-35 мл/кг охлажденного до 2-5°C 0,9% раствора натрия хлорида за максимально короткий срок. Что позволит снизить температуру тела больного приблизительно на 1°C. Как правило, больные после СЛР имеют определенную степень гиповолемии. И большинство пациентов, даже с кардиальной патологией, хорошо переносят этот объем инфузии. Но у больных с выраженной сердечной недостаточностью, при наличии почечного повреждения, введение столь больших объемов жидкости может быть противопоказано. В отделении надо иметь постоянный запас охлажденных до 2-5°C солевых растворов.
2. Используют другие доступные способы охлаждения:
- Обкладывают пациента, используя всю поверхность тела, пластиковыми мешками со снегом или льдом;
- Стараясь покрыть всю поверхность тела, используют пропитанные водой, а потом замороженные, полотенца, простыни;
- Проводят обдувание возможно большей поверхности тела охлажденным воздухом (бытовой кондиционер);
- Понятно, что если имеются штатные устройства поверхностного или внутрисосудистого охлаждения, используют их.
3. Измеряется центральная температура. Датчик для измерения температуры, в зависимости от его назначения, устанавливается в пищеводе, носоглотке или в наружном слуховом проходе или в мочевом пузыре. При снижении температуры тела до 33°C охлаждение прекращают. В дальнейшем колебания температуры стараются свести к минимуму – 1
Источник статьи: http://www.eurolab.ua/encyclopedia/ambulance/48870/